Пожалуй редко можно услышать об исследованиях красного мухомора и его алкалоидов. Однако изредка это происходит. В центре внимания – производное мусцимола (главного психоактивного действующего вещества мухомора красного), таинственный и уникальный габоксадол (THIP) - частичный агонист рецепторов ГАМКа и антагонист рецепторов ГАМКс.
Габоксадол был впервые синтезирован в 1977 году датским химиком Повлом Крогсгаард-Ларсеном, когда команда датских исследователей во главе с медицинским химиком и экспертом ГАМК начала синтезировать и испытывать десятки производных мусцимола.

До относительно недавнего времени самоэкспериментирование было жизненно важным компонентом открытия лекарств, и поэтому, когда Крогсгаард-Ларсен признал уникальность габоксадола, он начал принимать лекарство в увеличивающихся дозах, чтобы охарактеризовать его качественный эффект. «У нас постоянно брали образцы крови. Обычно я боюсь крови и мне не нравится боль от игл, но на этот раз я не испугался, и боли не было вообще. В 10 мг общее чувство, которое у меня было, когда я гулял, было таким, как будто я принял два или три пива - это было очень комфортное чувство».

Крогсгаард-Ларсен подал заявку на патент на габоксадол и передал его фармацевтической компании Lundbeck. Затем наступил всплеск испытаний на людях. В начале 1980-х годов препарат решили испытать в качестве анальгетика и анксиолитика (транквилизатора), а также в качестве средства для лечения поздней дискинезии, болезни Хантингтона, болезни Альцгеймера и спастичности. А в 1996 году начались серии клинических испытаний, спонсируемых фармацевтическими компаниями Lundbeck и Merck, в которых исследователи попытались использовать седативный эффект габоксадола для лечения бессонницы.

В отличие от всех известных традиционных снотворных препаратов, габоксадол имеет инновационный механизм действия осуществляющийся посредством взаимодействия исключительно с экстрасинаптическим подтипом ГАМК-рецепторов. Габоксадол продемонстрировал невиданный доселе механизм снотворного действия.
Он значительно отличается от действия бензодиазепинов, Z-препаратов (зопиклон, залеплон), барбитуратов, баклофена и других влияющих на ГАМК веществ. Большинство часто встречающихся ГАМКергических препаратов - валиум, амбиен, ксанакс, алкоголь - оказывают свое влияние на рецептор ГАМК, тем самым повышая эффективность ГАМК, уже циркулирующую естественным образом в мозге человека; но и мусцимол, и габоксадол оказывают свое влияние независимо от концентрации эндогенного ГАМК, заменяя нативный ГАМК на нейроне.
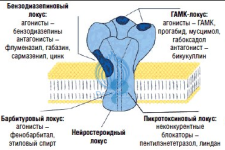
Компания Lundbeck заявляла, что габоксадол усиливает глубокий сон, но не так как это делают бензодиазепины. Испытуемые сообщали об улучшении интенсивности и качества сна, а также об улучшении производительности на следующий день. Еще в исследованиях 2000-ых годов было выявлено положительное действие подавления эпилептических приступов. Оказалось, что толерантность после приема габоксадола растет очень медленно и слабо по сравнению с другими ГАМК-препаратами.
Одно из исследований проходило с участием 14 пациентов с прогрессирующей стадией рака и пробным тестированием габоксадола как ненаркотического, не вызывающего привыкания анальгетика. Внутримышечные инъекции габоксадола оказались эффективными против злокачественной раковой боли, не вызывая проблем с дыханием, которые лежат в основе большинства смертельных исходов, связанных с опиатами. Пациенты отмечали эйфорию, ощущение, что он выпили «слишком много пива», и «ощущение закрытости» в голове. Двое ощутили такой сильный гипнотический эффект, что потеряли сознание.
Однако, не смотря на все эти чудесные открытия и реальные результаты, в марте 2007 года Merck и Lundbeck внезапно отменили работу над препаратом, сославшись на соображения безопасности и провал испытания эффективности. Надо признать, что габоксадол все же имел серьезные побочные эффекты, скорее интересные «психонавтам» и мешающие пациентам и врачам. Сообщалось о классических мухоморных или мусцимольных психотропных эффектах: эйфории, слуховых и зрительных галлюцинациях, диссоциации, беспокойстве, нарушении координации движений, расфокусировке зрения, различных ИСС.

Известно что при приеме от 10 до 30 мг, габоксадол действует как прекрасное седативное, анксиолитическое и снотворное средство, чаще без побочных эффектов, а вот начиная примерно с 35 мг вплоть до экспериментально использованных сумасшедших 160 мг, проявляется «психодел», само собой увеличивающийся с ростом дозировки.
В 2015 году Lundbeck продала свои права на габоксадол компании Ovid Therapeutics, чей план состоит в том, чтобы использовать препарат для лечения синдрома хрупкости X и синдрома Ангелмана («синдрома ангела»). Габоксадол там получил новое наименование - OV101.

Сообщение от Ovid Therapeutics и Angelman Syndrome Foundation:
"OV101, также называемый габоксадолом или THIP, представляет собой исследовательскую терапию, разработанную Ovid Therapeutics для лечения синдрома Ангельмана и синдрома хрупкости X.
OV101 - это небольшая молекула, полученная из соединения, называемого мусцимолом, которое естественным образом содержится в грибе (Amanita muscaria).
В сентябре 2016 года Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) присвоило орфанное лекарственное средство OV101 для лечения синдрома Ангелмана. В октябре 2017 года FDA расширило это обозначение для лечения синдрома хрупкости X. Овидий также получил два патента США (срок действия которых истекает в 2035 году) на методы лечения синдрома Ангелмана с использованием OV101.
Как работает OV101
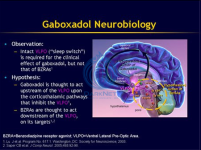
Это пероральный препарат, который избирательно активирует ГАМК-рецепторы, которые расположены на поверхности нервных клеток за пределами синапса. Синапс - это узкое пространство между двумя нервными клетками, где они общаются через химические мессенджеры, называемые нейротрансмиттерами.
ГАМК является нейротрансмиттером, который действует на два типа рецепторов: синаптические рецепторы (между нервами) и экстрасинаптические рецепторы (вдали от нервного окончания). OV101 специфически связывается с экстрасинаптическими рецепторами ГАМК.
ГАМК в основном подавляет чрезмерную активность нейронов, этот процесс называется тоническим торможением. Тоническое торможение важно, поскольку оно позволяет мозгу здорового человека правильно распознавать возбуждающие и тормозные неврологические сигналы без перегрузки.
Считается, что нарушение тонического торможения является основной причиной нарушений развития нервной системы, таких как синдромы Angelman и Fragile X. Эти расстройства в основном включают аномально сниженные уровни экстрасинаптической ГАМК, что в конечном итоге снижает тоническое торможение. Это приводит к тому, что мозг перегружается сигналами и, следовательно, теряет способность отличать важную информацию от фонового шума.
Селективное связывание OV101 с экстрасинаптическими рецепторами ГАМК восстанавливает тоническое торможение.
В доклинических исследованиях исследователи наблюдали, что OV101 улучшил симптомы синдромов Angelman и Fragile X.
OV101 в клинических испытаниях
Овидий успешно завершил фазу 1 клинического испытания (NCT03109756), в котором приняли участие семь мальчиков и пять девочек в возрасте от 13 до 17 лет, у которых был диагностирован синдром Ангельмана или Хрупкого Х. Это открытое исследование с применением одной дозы для одной дозы было разработано для оценки безопасности, толерантности и фармакокинетики OV101.
Результаты показали, что фармакокинетический профиль OV101 у подростков с синдромом Angelman и Fragile X был сходен с таковым, наблюдаемым у молодых людей. Они также продемонстрировали, что OV101 в целом безопасен и хорошо переносится.
Эти обнадеживающие результаты привели к включению подростков в продолжающееся исследование фазы 2 (NCT02996305), названное испытанием STARS, которое направлено на включение около 75 пациентов в возрасте от 13 до 49 лет с подтвержденным диагнозом синдрома Ангелмана.
Рандомизированное двойное слепое плацебо-контролируемое исследование направлено на оценку безопасности и переносимости OV101, а также его влияния на моторные навыки, дезадаптивное поведение, сон и качество жизни. Испытание вербует пациентов в Соединенных Штатах и Израиле и, как ожидается, завершится к ноябрю 2018 года."
Габоксадол был впервые синтезирован в 1977 году датским химиком Повлом Крогсгаард-Ларсеном, когда команда датских исследователей во главе с медицинским химиком и экспертом ГАМК начала синтезировать и испытывать десятки производных мусцимола.

До относительно недавнего времени самоэкспериментирование было жизненно важным компонентом открытия лекарств, и поэтому, когда Крогсгаард-Ларсен признал уникальность габоксадола, он начал принимать лекарство в увеличивающихся дозах, чтобы охарактеризовать его качественный эффект. «У нас постоянно брали образцы крови. Обычно я боюсь крови и мне не нравится боль от игл, но на этот раз я не испугался, и боли не было вообще. В 10 мг общее чувство, которое у меня было, когда я гулял, было таким, как будто я принял два или три пива - это было очень комфортное чувство».

Крогсгаард-Ларсен подал заявку на патент на габоксадол и передал его фармацевтической компании Lundbeck. Затем наступил всплеск испытаний на людях. В начале 1980-х годов препарат решили испытать в качестве анальгетика и анксиолитика (транквилизатора), а также в качестве средства для лечения поздней дискинезии, болезни Хантингтона, болезни Альцгеймера и спастичности. А в 1996 году начались серии клинических испытаний, спонсируемых фармацевтическими компаниями Lundbeck и Merck, в которых исследователи попытались использовать седативный эффект габоксадола для лечения бессонницы.

В отличие от всех известных традиционных снотворных препаратов, габоксадол имеет инновационный механизм действия осуществляющийся посредством взаимодействия исключительно с экстрасинаптическим подтипом ГАМК-рецепторов. Габоксадол продемонстрировал невиданный доселе механизм снотворного действия.
Он значительно отличается от действия бензодиазепинов, Z-препаратов (зопиклон, залеплон), барбитуратов, баклофена и других влияющих на ГАМК веществ. Большинство часто встречающихся ГАМКергических препаратов - валиум, амбиен, ксанакс, алкоголь - оказывают свое влияние на рецептор ГАМК, тем самым повышая эффективность ГАМК, уже циркулирующую естественным образом в мозге человека; но и мусцимол, и габоксадол оказывают свое влияние независимо от концентрации эндогенного ГАМК, заменяя нативный ГАМК на нейроне.

Компания Lundbeck заявляла, что габоксадол усиливает глубокий сон, но не так как это делают бензодиазепины. Испытуемые сообщали об улучшении интенсивности и качества сна, а также об улучшении производительности на следующий день. Еще в исследованиях 2000-ых годов было выявлено положительное действие подавления эпилептических приступов. Оказалось, что толерантность после приема габоксадола растет очень медленно и слабо по сравнению с другими ГАМК-препаратами.
Одно из исследований проходило с участием 14 пациентов с прогрессирующей стадией рака и пробным тестированием габоксадола как ненаркотического, не вызывающего привыкания анальгетика. Внутримышечные инъекции габоксадола оказались эффективными против злокачественной раковой боли, не вызывая проблем с дыханием, которые лежат в основе большинства смертельных исходов, связанных с опиатами. Пациенты отмечали эйфорию, ощущение, что он выпили «слишком много пива», и «ощущение закрытости» в голове. Двое ощутили такой сильный гипнотический эффект, что потеряли сознание.

Однако, не смотря на все эти чудесные открытия и реальные результаты, в марте 2007 года Merck и Lundbeck внезапно отменили работу над препаратом, сославшись на соображения безопасности и провал испытания эффективности. Надо признать, что габоксадол все же имел серьезные побочные эффекты, скорее интересные «психонавтам» и мешающие пациентам и врачам. Сообщалось о классических мухоморных или мусцимольных психотропных эффектах: эйфории, слуховых и зрительных галлюцинациях, диссоциации, беспокойстве, нарушении координации движений, расфокусировке зрения, различных ИСС.

Известно что при приеме от 10 до 30 мг, габоксадол действует как прекрасное седативное, анксиолитическое и снотворное средство, чаще без побочных эффектов, а вот начиная примерно с 35 мг вплоть до экспериментально использованных сумасшедших 160 мг, проявляется «психодел», само собой увеличивающийся с ростом дозировки.
В 2015 году Lundbeck продала свои права на габоксадол компании Ovid Therapeutics, чей план состоит в том, чтобы использовать препарат для лечения синдрома хрупкости X и синдрома Ангелмана («синдрома ангела»). Габоксадол там получил новое наименование - OV101.

Сообщение от Ovid Therapeutics и Angelman Syndrome Foundation:
"OV101, также называемый габоксадолом или THIP, представляет собой исследовательскую терапию, разработанную Ovid Therapeutics для лечения синдрома Ангельмана и синдрома хрупкости X.
OV101 - это небольшая молекула, полученная из соединения, называемого мусцимолом, которое естественным образом содержится в грибе (Amanita muscaria).
В сентябре 2016 года Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) присвоило орфанное лекарственное средство OV101 для лечения синдрома Ангелмана. В октябре 2017 года FDA расширило это обозначение для лечения синдрома хрупкости X. Овидий также получил два патента США (срок действия которых истекает в 2035 году) на методы лечения синдрома Ангелмана с использованием OV101.
Как работает OV101
Это пероральный препарат, который избирательно активирует ГАМК-рецепторы, которые расположены на поверхности нервных клеток за пределами синапса. Синапс - это узкое пространство между двумя нервными клетками, где они общаются через химические мессенджеры, называемые нейротрансмиттерами.
ГАМК является нейротрансмиттером, который действует на два типа рецепторов: синаптические рецепторы (между нервами) и экстрасинаптические рецепторы (вдали от нервного окончания). OV101 специфически связывается с экстрасинаптическими рецепторами ГАМК.
ГАМК в основном подавляет чрезмерную активность нейронов, этот процесс называется тоническим торможением. Тоническое торможение важно, поскольку оно позволяет мозгу здорового человека правильно распознавать возбуждающие и тормозные неврологические сигналы без перегрузки.
Считается, что нарушение тонического торможения является основной причиной нарушений развития нервной системы, таких как синдромы Angelman и Fragile X. Эти расстройства в основном включают аномально сниженные уровни экстрасинаптической ГАМК, что в конечном итоге снижает тоническое торможение. Это приводит к тому, что мозг перегружается сигналами и, следовательно, теряет способность отличать важную информацию от фонового шума.
Селективное связывание OV101 с экстрасинаптическими рецепторами ГАМК восстанавливает тоническое торможение.
В доклинических исследованиях исследователи наблюдали, что OV101 улучшил симптомы синдромов Angelman и Fragile X.
OV101 в клинических испытаниях
Овидий успешно завершил фазу 1 клинического испытания (NCT03109756), в котором приняли участие семь мальчиков и пять девочек в возрасте от 13 до 17 лет, у которых был диагностирован синдром Ангельмана или Хрупкого Х. Это открытое исследование с применением одной дозы для одной дозы было разработано для оценки безопасности, толерантности и фармакокинетики OV101.
Результаты показали, что фармакокинетический профиль OV101 у подростков с синдромом Angelman и Fragile X был сходен с таковым, наблюдаемым у молодых людей. Они также продемонстрировали, что OV101 в целом безопасен и хорошо переносится.
Эти обнадеживающие результаты привели к включению подростков в продолжающееся исследование фазы 2 (NCT02996305), названное испытанием STARS, которое направлено на включение около 75 пациентов в возрасте от 13 до 49 лет с подтвержденным диагнозом синдрома Ангелмана.
Рандомизированное двойное слепое плацебо-контролируемое исследование направлено на оценку безопасности и переносимости OV101, а также его влияния на моторные навыки, дезадаптивное поведение, сон и качество жизни. Испытание вербует пациентов в Соединенных Штатах и Израиле и, как ожидается, завершится к ноябрю 2018 года."
