Помню с восторгом читал предположения Шульгина о химическом воздействии на растения для получения нужных компонентов в составе, но генная инженерия — это фантастика, которую мы заждались!
Встречайте!
*Кокаин в ГМО листьях табака*
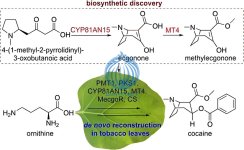
Группа исследователей Китайской академии наук совместно с коллегой из Международного исследовательского центра Syngenta Jealott Hill в Великобритании разработала способ синтеза кокаина с использованием табачного растения. Группа описывает, как они синтезировали печально известное лекарство, и возможные варианты использования этого процесса в своей статье, опубликованной в журнале Американского химического общества.
Поскольку выращивание растений коки для производства кокаина требует много труда, ученые на протяжении последнего столетия искали способ производить его в лаборатории. К сожалению, такие усилия оказались бесплодными из-за сложной биохимии растения коки и его ценного побочного продукта. Теперь, в этой новой работе, исследователи не только выяснили биохимию растения и кокаина, который оно производит, но и синтезировали небольшое количество кокаина путем генной инженерии типа табачного растения для производства материала в его листьях.
Чтобы доказать свое открытие, группа генетически модифицировала растение табака для производства двух ферментов в его листьях, что привело к производству небольшого количества кокаина (с помощью вещества, которое также вырабатывается в растении под названием орнитин, которое похоже на предшественника в растении коки).
Исследователи отмечают, что их усилия были сосредоточены на синтезе кокаина для его использования в медицинских целях, таких как обезболивание. Кроме того, процесс, который они использовали для производства кокаина на табачных растениях, слишком технически сложный для использования преступниками, решившими производить наркотик незаконно.
*Псилоцибин в ГМО дрожжах*
Психоделики в настоящее время на волне положительного импульса, вызванного каннабисом, и если псилоцибин будет одобрен в качестве фармацевтического препарата, производство в дрожжах, по-видимому, является наиболее коммерчески жизнеспособным вариантом.
"Слишком дорого извлекать псилоцибин из магических грибов, а лучшие методы химического синтеза требуют дорогостоящих и трудных для источника запуска субстратов. Таким образом, необходимо снизить стоимость производства и обеспечить более последовательную цепочку поставок" — говорит Ник Милн, бывший постдок в DTU Biosustain и CSO и соучредитель Octarine Bio.
Производства псилоцибина таким способом вызвали большой интерес и исследователи уже доказали мелкое производство в E. coli. Однако производство бактерий сопровождается широким спектром проблем, которые могут быть решены с помощью дрожжей.
С использованием дрожжей ученые доказывают, что псилоцибин может быть произведен de novo, что означает, что вы можете производить молекулу, просто выращивая дрожжи с сахаром и другими питательными веществами, без необходимости добавления каких-либо других стартовых субстратов.
Производство псилоцибина de novo в E. coli затруднено, так как ключевой фермент не работает у бактерий, и поэтому, чтобы обойти эту проблему, вам нужно добавить дорогой стартовый субстрат, что делает весь производственный процесс слишком дорогостоящим.
"Поскольку дрожжевые и грибы Псилоцибы являются довольно тесно связанными видами, этот фермент очень хорошо работает в дрожжах, обеспечивая гораздо более экономическую альтернативу", — говорит руководитель группы DTU Biosustain Irina Borodina.
В исследовании, опубликованном в Metabolic Engineering Journal, исследователи достигли довольно высоких показателей, но если производство должно быть расширено, необходимо преодолеть одно серьезное препятствие.
На скелете ядра псилоцибина находится фосфатная группа, которая расщепляется, когда молекула преобразуется в его активную форму.
"Что мы находим в исследовании? То, что мы получаем много этого не фосфорилированного соединения псилоцина. По сути, мы теряем половину нашего продукта, потому что группа фосфатов отпадает. Работа с этим большим количеством псилоцина — это то, что абсолютно необходимо решить, прежде чем реально перейти к производственному процессу", — объясняет Ник Милн.
В то время как производство de novo псилоцибина в дрожжах в этих титрах следует считать впечатляющим доказательством концепции, исследователи, стоящие за исследованием, также подчеркивают важность производства других новых производных.
Грибы Psilocybe также производят ряд молекул, которые структурно похожи на псилоцибин, но их слишком трудно очищать, что затрудняет исследование их терапевтического эффекта. В этом исследовании исследователи продемонстрировали производство ряда производных пути псилоцибина, и далее, сочетая гены из биосинтетического пути мелатонина, может продемонстрировать производство совершенно новой молекулы.
Эта технология была передана Octarine Bio, компании из The Novo Nordisk Foundation Center for Biosustain (DTU Biosustain) и Копенгагенскому университету, которые заинтересованы не только в крупномасштабном производстве псилоцибина, но и потенциале производства новых производных.
"Наш интерес заключается не только в том, чтобы сделать производство псилоцибина килограммами, но и в использовании биологического оборудования для того, чтобы сделать новые производные, которые не доступны сегодня. Таким образом, очень полезно, что мы могли не только продемонстрировать производство псилоцибина, но и найти много производных, которые могут оказаться имеющими важное терапевтическое значение", — говорит Ник Милн.
Ну что скоро новые синтетические аналоги псицолоцибина на основе производных полученных из ГМО дрожжей, увидим на рынке?
*Восстановление полного биосинтеза D - лизергиновой кислоты в дрожжах*
Алкалоиды спорыньи широко использовались в качестве терапевтических средств на протяжении всей истории. Фармакологический эффект алкалоидов спорыньи приписывают молекулярному сходству между эрголиновым скелетом и моноаминовыми нейротрансмиттерами, такими как адреналин, дофамин и серотонин. Алкалоиды спорыньи и их синтетические производные широко используются в современной медицине для лечения ряда неврологических заболеваний, таких как паркинсонизм, деменция и гипертония.
Фармакофор эрголина является важной основой для потенциальных терапевтических открытий и разработок, особенно при лечении неврологических и психических расстройств. Например, диэтиламид D -лизергиновой кислоты (LSD), химически полученный алкалоид спорыньи, является одним из наиболее мощных агонистов 5-HT 2A серотонинергического рецептора. Ключевым активным фармацевтическим ингредиентом (API) этих производных эрголина является D -лизергиновая кислота (DLA).
Предполагается, что биосинтез DLA с использованием промышленно пригодных микроорганизмов, таких как пекарские дрожжи, вероятно, позволит обойти ключевые проблемы с текущими методами производства.
Эта работа основывается на растущем количестве работ, демонстрирующих использование пригодных для промышленного использования микроорганизмов для производства сложных натуральных продуктов с использованием экономичного и возобновляемого сырья, например, то, что было сделано для биосинтеза опиоидов. Сконструированные штаммы обеспечивают отличную платформу для открытия полусинтетических терапевтических ведущих соединений, а также для разработки экспериментальных штаммов для производства важных терапевтических средств природного происхождения.
Наконец, с недавним возрождением исследований по перепрофилированию психоделических соединений для применения в качестве антидепрессантов и анксиолитиков, мы считаем, что наш штамм может быть использован для поддержки усилий по исследованию природного и полусинтетического химического пространства терапевтических средств на основе эрголина. для выявления направлений с повышенным терапевтическим потенциалом и меньшим количеством побочных эффектов.
*Каннабиноиды в дрожжах*
Синтетические биологи Калифорнийского университета в Беркли разработали пивные дрожжи для производства основных ингредиентов марихуаны — изменяющего сознание ТГК и не психоактивного КБД, а также новых каннабиноидов, которых нет в самом растении.
Питаясь только сахаром, дрожжи представляют собой простой и дешевый способ производства чистых каннабиноидов, которые сегодня дорого извлекать из почек растения марихуаны Cannabis sativa.
«Для потребителя преимущества заключаются в высококачественных, недорогих КБД и ТГК: вы получаете именно то, что хотите от дрожжей», — сказал Джей Кислинг, профессор химической и биомолекулярной инженерии и биоинженерии Калифорнийского университета в Беркли, а также научный сотрудник факультета Национальная лаборатория Лоуренса Беркли. «Это более безопасный и экологически чистый способ производства каннабиноидов».
Каннабис и его экстракты, в том числе высокоиндуцирующий ТГК или тетрагидроканнабинол, в настоящее время легальны в 10 штатах и округе Колумбия, а рекреационная марихуана — курение, вейпинг или употребление в пищу — представляет собой многомиллиардный бизнес по всей стране. Лекарства, содержащие ТГК, были одобрены Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов для уменьшения тошноты после химиотерапии и улучшения аппетита у больных СПИДом.
CBD, или каннабидиол, все чаще используется в косметике — так называемых космецевтиках — и был одобрен для лечения детских эпилептических припадков. Его исследуют в качестве терапии многих состояний, включая тревогу, болезнь Паркинсона и хроническую боль.
Но медицинские исследования более чем 100 других химических веществ в марихуане были трудными, потому что химические вещества встречаются в крошечных количествах, что затрудняет их извлечение из растения. Недорогие, более чистые источники, такие как дрожжи, могут облегчить такие исследования.
Кроме того, добавил он, существует «возможность новых методов лечения, основанных на новых каннабиноидах: редких, которые почти невозможно получить из растения. Или неестественных, которые невозможно получить из растения».
*Почти одновременно с этой работой вышло исследование синтеза ТГК из дрожжей Текилы*
Немецкая фармацевтическая компания Farmako подала заявку на патент на свой процесс, в котором используются генетически модифицированные бактерии текилы для производства каннабиноидов из сахара, что значительно снижает стоимость производства таких веществ, как ТГК.
Она утверждает, что её производственный процесс может значительно сократить затраты на производство каннабиноидов, сэкономив деньги отрасли и способствуя дешевому производству в промышленных масштабах.
В нем утверждается, что 1 килограмм ТГК — каннабиноида, также известного как тетрагидроканнабинол, — будет стоить примерно на одну тысячную меньше при использовании процесса биосинтеза.
* дрожжи с гиосциамином и скополамином*
Исходя из простых сахаров и аминокислот объединили функциональную геномику, чтобы идентифицировать отсутствующий фермент пути, белковую инженерию, чтобы обеспечить функциональную экспрессию ацилтрансферазы посредством доставки в вакуоль, гетерологичные транспортеры для облегчения внутриклеточной маршрутизации и оптимизацию штамма для улучшения титров. Интегрированная система размещает более двадцати белков, адаптированных из дрожжей, бактерий, растений и животных, в шести субклеточных местах, чтобы резюмировать пространственную организацию биосинтеза тропановых алкалоидов в растениях. Платформы микробного биосинтеза могут способствовать открытию производных тропановых алкалоидов в качестве новых терапевтических средств для лечения неврологических заболеваний и, как только они будут масштабированы, обеспечат надежные и оперативные поставки этих основных лекарственных средств.
a. Конструирование модульного пути биосинтеза скополамина в дрожжах.
Цветовая схема фермент/белок: оранжевый, дрожжевой (сверхэкспрессированный);
зеленый, растение;
фиолетовый, бактерии;
красный, другой эукариот;
серый, спонтанный/неферментативный.
Красные прямоугольники указывают на разрушенные дрожжевые белки;
пунктирные или сплошные линии мембран вакуолей очерчивают функциональные биосинтетические модули.
DsRed– Ab LS, Discosoma sp.
красный флуоресцентный белок, слитый с N-концом A. belladonna литторинсинтазы
b.продукция PLA в дрожжах, сконструированных для экспрессии PPR или LDH. Гетерологичные ферменты или отрицательный контроль (BFP) экспрессировали из низкокопийных плазмид в штамме CSY1251. c , Мониторинг множественных реакций (MRM) и извлеченные следы ионной хроматограммы (EIC) из культуральной среды дрожжей, сконструированных для поэтапного восстановления биосинтеза глюкозида PLA с помощью модуля III. Следы хроматограммы являются репрезентативными для трех биологических повторов. d , Относительные титры глюкозида PLA в дрожжах, сконструированных для сверхэкспрессии ферментов биосинтеза UDP-глюкозы. Ферменты или отрицательный контроль (BFP) экспрессировали из низкокопийных плазмид в штамме CSY1288. e , относительные титры глюкозидов PLA в CSY1288 с нарушениями эндогенных глюкозидаз. В d и e накопление глюкозида PLA сравнивали с использованием относительных титров из-за отсутствия аутентичного химического стандарта. Штаммы культивировали в течение 72 часов перед анализом метаболитов в культуральном супернатанте с помощью жидкостной хроматографии и тандемной масс-спектрометрии (ЖХ-МС/МС). Данные в b , d и e представляют собой среднее значение n = 3 биологически независимых образцов (открытые кружки), планки погрешностей обозначают sd * P <0,05, ** P <0,01, *** P Стьюдента <0,001, двустороннее t - контрольная работа. Статистическая значимость показана относительно контроля.
*Опиойды в дрожжах*
Обычный кишечный микроб скоро сможет предложить нам обезболивающее. Японские биоинженеры модифицировали гены Escherichia coli таким образом, чтобы они выкачивали тебаин, предшественник морфина, который можно модифицировать для создания болеутоляющих средств. Генетически модифицированная кишечная палочка производит в 300 раз больше тебаина с минимальным риском неконтролируемого использования по сравнению с недавно разработанным методом с использованием дрожжей.
«Морфин имеет сложную молекулярную структуру, из-за этого производство морфина и подобных обезболивающих является дорогостоящим и трудоемким», — сказал автор исследования Фумихико Сато из Киотского университета.
«Но с нашей кишечной палочкой мы смогли получить 2,1 миллиграмма тебаина в течение нескольких дней из примерно 20 граммов сахара».
Морфин извлекается из макового сока в процессе, в результате которого получаются опиаты, такие как тебаин и кодеин. Другие биологи-синтетики недавно сконструировали геном дрожжей таким образом, чтобы они производили опиоидные алкалоиды из сахара. Однако существовали этические проблемы, в том числе риск того, что обезболивающие молекулы могут быть легко и нерегулируемо произведены при условии, что у человека есть доступ к необходимому штамму дрожжей.
Сато говорит, что в отношении E. coli такой производственный риск незначителен.
четыре штамма генетически модифицированной кишечной палочки «Для превращения сахара в тебаин необходимы », — объясняет Сато. « С E. coli труднее справиться, и для этого требуется опыт. Это должно послужить сдерживающим фактором для нерегулируемого производства».
В 2011 году Сато и его коллеги сконструировали E. coli для синтеза ретикулина, еще одного предшественника морфина, который появляется в процессе трансформации раньше, чем тебаин. В новую систему команда добавила гены других бактерий и гены ферментов опийного мака, коптиса японского и арабидопсиса . Команда считает, что высокая активность ферментов в новой системе способствовала их успеху в производстве тебаина, и надеется добиться дальнейших улучшений.
«Добавив еще два гена, наша кишечная палочка смогла производить гидрокодон, что, безусловно, повысит практичность этого метода», — сказал Сато. «С еще несколькими улучшениями в технике и соблюдением фармацевтических правил производство морфиноподобных болеутоляющих средств из микробов вскоре может стать реальностью».
Встречайте!
*Кокаин в ГМО листьях табака*
Группа исследователей Китайской академии наук совместно с коллегой из Международного исследовательского центра Syngenta Jealott Hill в Великобритании разработала способ синтеза кокаина с использованием табачного растения. Группа описывает, как они синтезировали печально известное лекарство, и возможные варианты использования этого процесса в своей статье, опубликованной в журнале Американского химического общества.
Поскольку выращивание растений коки для производства кокаина требует много труда, ученые на протяжении последнего столетия искали способ производить его в лаборатории. К сожалению, такие усилия оказались бесплодными из-за сложной биохимии растения коки и его ценного побочного продукта. Теперь, в этой новой работе, исследователи не только выяснили биохимию растения и кокаина, который оно производит, но и синтезировали небольшое количество кокаина путем генной инженерии типа табачного растения для производства материала в его листьях.
Чтобы доказать свое открытие, группа генетически модифицировала растение табака для производства двух ферментов в его листьях, что привело к производству небольшого количества кокаина (с помощью вещества, которое также вырабатывается в растении под названием орнитин, которое похоже на предшественника в растении коки).
Исследователи отмечают, что их усилия были сосредоточены на синтезе кокаина для его использования в медицинских целях, таких как обезболивание. Кроме того, процесс, который они использовали для производства кокаина на табачных растениях, слишком технически сложный для использования преступниками, решившими производить наркотик незаконно.
*Псилоцибин в ГМО дрожжах*
Психоделики в настоящее время на волне положительного импульса, вызванного каннабисом, и если псилоцибин будет одобрен в качестве фармацевтического препарата, производство в дрожжах, по-видимому, является наиболее коммерчески жизнеспособным вариантом.
"Слишком дорого извлекать псилоцибин из магических грибов, а лучшие методы химического синтеза требуют дорогостоящих и трудных для источника запуска субстратов. Таким образом, необходимо снизить стоимость производства и обеспечить более последовательную цепочку поставок" — говорит Ник Милн, бывший постдок в DTU Biosustain и CSO и соучредитель Octarine Bio.
Производства псилоцибина таким способом вызвали большой интерес и исследователи уже доказали мелкое производство в E. coli. Однако производство бактерий сопровождается широким спектром проблем, которые могут быть решены с помощью дрожжей.
С использованием дрожжей ученые доказывают, что псилоцибин может быть произведен de novo, что означает, что вы можете производить молекулу, просто выращивая дрожжи с сахаром и другими питательными веществами, без необходимости добавления каких-либо других стартовых субстратов.
Производство псилоцибина de novo в E. coli затруднено, так как ключевой фермент не работает у бактерий, и поэтому, чтобы обойти эту проблему, вам нужно добавить дорогой стартовый субстрат, что делает весь производственный процесс слишком дорогостоящим.
"Поскольку дрожжевые и грибы Псилоцибы являются довольно тесно связанными видами, этот фермент очень хорошо работает в дрожжах, обеспечивая гораздо более экономическую альтернативу", — говорит руководитель группы DTU Biosustain Irina Borodina.
В исследовании, опубликованном в Metabolic Engineering Journal, исследователи достигли довольно высоких показателей, но если производство должно быть расширено, необходимо преодолеть одно серьезное препятствие.
На скелете ядра псилоцибина находится фосфатная группа, которая расщепляется, когда молекула преобразуется в его активную форму.
"Что мы находим в исследовании? То, что мы получаем много этого не фосфорилированного соединения псилоцина. По сути, мы теряем половину нашего продукта, потому что группа фосфатов отпадает. Работа с этим большим количеством псилоцина — это то, что абсолютно необходимо решить, прежде чем реально перейти к производственному процессу", — объясняет Ник Милн.
В то время как производство de novo псилоцибина в дрожжах в этих титрах следует считать впечатляющим доказательством концепции, исследователи, стоящие за исследованием, также подчеркивают важность производства других новых производных.
Грибы Psilocybe также производят ряд молекул, которые структурно похожи на псилоцибин, но их слишком трудно очищать, что затрудняет исследование их терапевтического эффекта. В этом исследовании исследователи продемонстрировали производство ряда производных пути псилоцибина, и далее, сочетая гены из биосинтетического пути мелатонина, может продемонстрировать производство совершенно новой молекулы.
Эта технология была передана Octarine Bio, компании из The Novo Nordisk Foundation Center for Biosustain (DTU Biosustain) и Копенгагенскому университету, которые заинтересованы не только в крупномасштабном производстве псилоцибина, но и потенциале производства новых производных.
"Наш интерес заключается не только в том, чтобы сделать производство псилоцибина килограммами, но и в использовании биологического оборудования для того, чтобы сделать новые производные, которые не доступны сегодня. Таким образом, очень полезно, что мы могли не только продемонстрировать производство псилоцибина, но и найти много производных, которые могут оказаться имеющими важное терапевтическое значение", — говорит Ник Милн.
Ну что скоро новые синтетические аналоги псицолоцибина на основе производных полученных из ГМО дрожжей, увидим на рынке?
*Восстановление полного биосинтеза D - лизергиновой кислоты в дрожжах*
Алкалоиды спорыньи широко использовались в качестве терапевтических средств на протяжении всей истории. Фармакологический эффект алкалоидов спорыньи приписывают молекулярному сходству между эрголиновым скелетом и моноаминовыми нейротрансмиттерами, такими как адреналин, дофамин и серотонин. Алкалоиды спорыньи и их синтетические производные широко используются в современной медицине для лечения ряда неврологических заболеваний, таких как паркинсонизм, деменция и гипертония.
Фармакофор эрголина является важной основой для потенциальных терапевтических открытий и разработок, особенно при лечении неврологических и психических расстройств. Например, диэтиламид D -лизергиновой кислоты (LSD), химически полученный алкалоид спорыньи, является одним из наиболее мощных агонистов 5-HT 2A серотонинергического рецептора. Ключевым активным фармацевтическим ингредиентом (API) этих производных эрголина является D -лизергиновая кислота (DLA).
Предполагается, что биосинтез DLA с использованием промышленно пригодных микроорганизмов, таких как пекарские дрожжи, вероятно, позволит обойти ключевые проблемы с текущими методами производства.
Эта работа основывается на растущем количестве работ, демонстрирующих использование пригодных для промышленного использования микроорганизмов для производства сложных натуральных продуктов с использованием экономичного и возобновляемого сырья, например, то, что было сделано для биосинтеза опиоидов. Сконструированные штаммы обеспечивают отличную платформу для открытия полусинтетических терапевтических ведущих соединений, а также для разработки экспериментальных штаммов для производства важных терапевтических средств природного происхождения.
Наконец, с недавним возрождением исследований по перепрофилированию психоделических соединений для применения в качестве антидепрессантов и анксиолитиков, мы считаем, что наш штамм может быть использован для поддержки усилий по исследованию природного и полусинтетического химического пространства терапевтических средств на основе эрголина. для выявления направлений с повышенным терапевтическим потенциалом и меньшим количеством побочных эффектов.
*Каннабиноиды в дрожжах*
Синтетические биологи Калифорнийского университета в Беркли разработали пивные дрожжи для производства основных ингредиентов марихуаны — изменяющего сознание ТГК и не психоактивного КБД, а также новых каннабиноидов, которых нет в самом растении.
Питаясь только сахаром, дрожжи представляют собой простой и дешевый способ производства чистых каннабиноидов, которые сегодня дорого извлекать из почек растения марихуаны Cannabis sativa.
«Для потребителя преимущества заключаются в высококачественных, недорогих КБД и ТГК: вы получаете именно то, что хотите от дрожжей», — сказал Джей Кислинг, профессор химической и биомолекулярной инженерии и биоинженерии Калифорнийского университета в Беркли, а также научный сотрудник факультета Национальная лаборатория Лоуренса Беркли. «Это более безопасный и экологически чистый способ производства каннабиноидов».
Каннабис и его экстракты, в том числе высокоиндуцирующий ТГК или тетрагидроканнабинол, в настоящее время легальны в 10 штатах и округе Колумбия, а рекреационная марихуана — курение, вейпинг или употребление в пищу — представляет собой многомиллиардный бизнес по всей стране. Лекарства, содержащие ТГК, были одобрены Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов для уменьшения тошноты после химиотерапии и улучшения аппетита у больных СПИДом.
CBD, или каннабидиол, все чаще используется в косметике — так называемых космецевтиках — и был одобрен для лечения детских эпилептических припадков. Его исследуют в качестве терапии многих состояний, включая тревогу, болезнь Паркинсона и хроническую боль.
Но медицинские исследования более чем 100 других химических веществ в марихуане были трудными, потому что химические вещества встречаются в крошечных количествах, что затрудняет их извлечение из растения. Недорогие, более чистые источники, такие как дрожжи, могут облегчить такие исследования.
Кроме того, добавил он, существует «возможность новых методов лечения, основанных на новых каннабиноидах: редких, которые почти невозможно получить из растения. Или неестественных, которые невозможно получить из растения».
*Почти одновременно с этой работой вышло исследование синтеза ТГК из дрожжей Текилы*
Немецкая фармацевтическая компания Farmako подала заявку на патент на свой процесс, в котором используются генетически модифицированные бактерии текилы для производства каннабиноидов из сахара, что значительно снижает стоимость производства таких веществ, как ТГК.
Она утверждает, что её производственный процесс может значительно сократить затраты на производство каннабиноидов, сэкономив деньги отрасли и способствуя дешевому производству в промышленных масштабах.
В нем утверждается, что 1 килограмм ТГК — каннабиноида, также известного как тетрагидроканнабинол, — будет стоить примерно на одну тысячную меньше при использовании процесса биосинтеза.
* дрожжи с гиосциамином и скополамином*
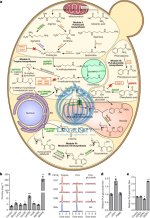
Исходя из простых сахаров и аминокислот объединили функциональную геномику, чтобы идентифицировать отсутствующий фермент пути, белковую инженерию, чтобы обеспечить функциональную экспрессию ацилтрансферазы посредством доставки в вакуоль, гетерологичные транспортеры для облегчения внутриклеточной маршрутизации и оптимизацию штамма для улучшения титров. Интегрированная система размещает более двадцати белков, адаптированных из дрожжей, бактерий, растений и животных, в шести субклеточных местах, чтобы резюмировать пространственную организацию биосинтеза тропановых алкалоидов в растениях. Платформы микробного биосинтеза могут способствовать открытию производных тропановых алкалоидов в качестве новых терапевтических средств для лечения неврологических заболеваний и, как только они будут масштабированы, обеспечат надежные и оперативные поставки этих основных лекарственных средств.
a. Конструирование модульного пути биосинтеза скополамина в дрожжах.
Цветовая схема фермент/белок: оранжевый, дрожжевой (сверхэкспрессированный);
зеленый, растение;
фиолетовый, бактерии;
красный, другой эукариот;
серый, спонтанный/неферментативный.
Красные прямоугольники указывают на разрушенные дрожжевые белки;
пунктирные или сплошные линии мембран вакуолей очерчивают функциональные биосинтетические модули.
DsRed– Ab LS, Discosoma sp.
красный флуоресцентный белок, слитый с N-концом A. belladonna литторинсинтазы
b.продукция PLA в дрожжах, сконструированных для экспрессии PPR или LDH. Гетерологичные ферменты или отрицательный контроль (BFP) экспрессировали из низкокопийных плазмид в штамме CSY1251. c , Мониторинг множественных реакций (MRM) и извлеченные следы ионной хроматограммы (EIC) из культуральной среды дрожжей, сконструированных для поэтапного восстановления биосинтеза глюкозида PLA с помощью модуля III. Следы хроматограммы являются репрезентативными для трех биологических повторов. d , Относительные титры глюкозида PLA в дрожжах, сконструированных для сверхэкспрессии ферментов биосинтеза UDP-глюкозы. Ферменты или отрицательный контроль (BFP) экспрессировали из низкокопийных плазмид в штамме CSY1288. e , относительные титры глюкозидов PLA в CSY1288 с нарушениями эндогенных глюкозидаз. В d и e накопление глюкозида PLA сравнивали с использованием относительных титров из-за отсутствия аутентичного химического стандарта. Штаммы культивировали в течение 72 часов перед анализом метаболитов в культуральном супернатанте с помощью жидкостной хроматографии и тандемной масс-спектрометрии (ЖХ-МС/МС). Данные в b , d и e представляют собой среднее значение n = 3 биологически независимых образцов (открытые кружки), планки погрешностей обозначают sd * P <0,05, ** P <0,01, *** P Стьюдента <0,001, двустороннее t - контрольная работа. Статистическая значимость показана относительно контроля.
*Опиойды в дрожжах*
Обычный кишечный микроб скоро сможет предложить нам обезболивающее. Японские биоинженеры модифицировали гены Escherichia coli таким образом, чтобы они выкачивали тебаин, предшественник морфина, который можно модифицировать для создания болеутоляющих средств. Генетически модифицированная кишечная палочка производит в 300 раз больше тебаина с минимальным риском неконтролируемого использования по сравнению с недавно разработанным методом с использованием дрожжей.
«Морфин имеет сложную молекулярную структуру, из-за этого производство морфина и подобных обезболивающих является дорогостоящим и трудоемким», — сказал автор исследования Фумихико Сато из Киотского университета.
«Но с нашей кишечной палочкой мы смогли получить 2,1 миллиграмма тебаина в течение нескольких дней из примерно 20 граммов сахара».
Морфин извлекается из макового сока в процессе, в результате которого получаются опиаты, такие как тебаин и кодеин. Другие биологи-синтетики недавно сконструировали геном дрожжей таким образом, чтобы они производили опиоидные алкалоиды из сахара. Однако существовали этические проблемы, в том числе риск того, что обезболивающие молекулы могут быть легко и нерегулируемо произведены при условии, что у человека есть доступ к необходимому штамму дрожжей.
Сато говорит, что в отношении E. coli такой производственный риск незначителен.
четыре штамма генетически модифицированной кишечной палочки «Для превращения сахара в тебаин необходимы », — объясняет Сато. « С E. coli труднее справиться, и для этого требуется опыт. Это должно послужить сдерживающим фактором для нерегулируемого производства».
В 2011 году Сато и его коллеги сконструировали E. coli для синтеза ретикулина, еще одного предшественника морфина, который появляется в процессе трансформации раньше, чем тебаин. В новую систему команда добавила гены других бактерий и гены ферментов опийного мака, коптиса японского и арабидопсиса . Команда считает, что высокая активность ферментов в новой системе способствовала их успеху в производстве тебаина, и надеется добиться дальнейших улучшений.
«Добавив еще два гена, наша кишечная палочка смогла производить гидрокодон, что, безусловно, повысит практичность этого метода», — сказал Сато. «С еще несколькими улучшениями в технике и соблюдением фармацевтических правил производство морфиноподобных болеутоляющих средств из микробов вскоре может стать реальностью».